
找答案
首页>高中化学>能量的相互转化考试题目
【简答题】
(12分)工业上合成甲醇一般采用下列反应:
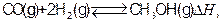 下表是该反应在不同温度下的化学平衡常数(K):
下表是该反应在不同温度下的化学平衡常数(K):
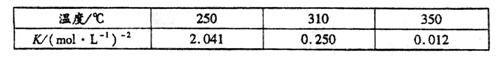 (1)由表中数据判断
(1)由表中数据判断
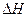 0(填“>”、“=”或“<”)。 (2)某温度下,将2molCO和6molH 2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L -1,则此时的温度为 ℃。 (3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
0(填“>”、“=”或“<”)。 (2)某温度下,将2molCO和6molH 2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L -1,则此时的温度为 ℃。 (3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
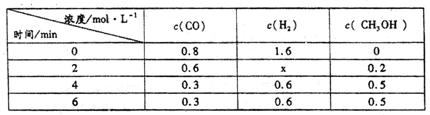 ①反应从2min到4min之间,H 2的反应速率为 。 ②反应达到平衡时CO的转化率为 。 ③反应在第2min时改变了反应条件,改变的条件可能是 (填序号)。 a.使用催化剂 b.降低温度 c.增加H 2的浓度 (4)常温常压
①反应从2min到4min之间,H 2的反应速率为 。 ②反应达到平衡时CO的转化率为 。 ③反应在第2min时改变了反应条件,改变的条件可能是 (填序号)。 a.使用催化剂 b.降低温度 c.增加H 2的浓度 (4)常温常压
 下: ①
下: ①
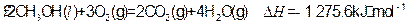 ②
②
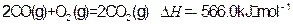 ③
③
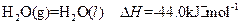 写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: (5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳。该电池的负极反应式为: 。 若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H 2体积(标况)为 L。
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: (5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳。该电池的负极反应式为: 。 若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H 2体积(标况)为 L。
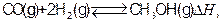 下表是该反应在不同温度下的化学平衡常数(K):
下表是该反应在不同温度下的化学平衡常数(K):
 (1)由表中数据判断
(1)由表中数据判断
 0(填“>”、“=”或“<”)。 (2)某温度下,将2molCO和6molH 2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L -1,则此时的温度为 ℃。 (3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
0(填“>”、“=”或“<”)。 (2)某温度下,将2molCO和6molH 2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L -1,则此时的温度为 ℃。 (3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
 ①反应从2min到4min之间,H 2的反应速率为 。 ②反应达到平衡时CO的转化率为 。 ③反应在第2min时改变了反应条件,改变的条件可能是 (填序号)。 a.使用催化剂 b.降低温度 c.增加H 2的浓度 (4)常温常压
①反应从2min到4min之间,H 2的反应速率为 。 ②反应达到平衡时CO的转化率为 。 ③反应在第2min时改变了反应条件,改变的条件可能是 (填序号)。 a.使用催化剂 b.降低温度 c.增加H 2的浓度 (4)常温常压
 下: ①
下: ①
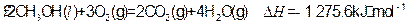 ②
②
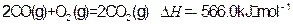 ③
③
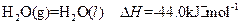 写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: (5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳。该电池的负极反应式为: 。 若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H 2体积(标况)为 L。
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: (5)一种甲醇燃料电池中发生的化学反应为:在酸性溶液中甲醇与氧化作用生成水和二氧化碳。该电池的负极反应式为: 。 若以上述燃料电池为电源来电解饱和食盐水,当消耗32g甲醇时,电解产生的H 2体积(标况)为 L。参考答案:
登录免费查看参考答案
参考解析:
登录免费查看参考解析
知识点:
登录免费查看知识点
答题技巧:
登录免费查看答题技巧
被用于:
暂无被用于


刷刷题刷刷变学霸
相关题目:
【简答题】Fe、H2O、H2、O2、KMnO4五种物质,按要求写出反应的化学方程式.(1)两个化合反应:_________、___________(2)两个分解反应:_______、____________.
【单选题】在温度压强不变的情况下,已知N 2O 4 2NO 2,2mol N 2O 4在密闭容器内分解成NO 2,到达平衡时生成了0.6mol NO 2,则平衡时气体的总物质的量是( )
【简答题】(13分)已知短周期主族元素X、Y、Z、W,原子序数依次增大且X和Y的原子序数之和等于Z的原子序数,X和Z可形成X 2 Z,X 2 Z 2 两种化合物,W是短周期主族元素中半径最大的元素。 (1)W在周期表中的位置: 。 (2)在一定条件下,容积为1L密闭容器中加入1.2molX 2 和0.4molY 2 ,发生如下反应: 3X 2 (g) + Y 2 (g) 2YX 3 (g) △ H 反应各...
【单选题】将25℃、101.3kPa、1.0LO2和0℃、202.6kPa、2.0LH2以及-60℃、303.9kPa、3.0LN2充入2.0L密闭容器中,温度保持在25℃,则( )。
【简答题】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用.工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)⇌CH3OCH3(g)+3H2O(g)已知该反应平衡常数(K)与温度(T)的关系如图所示.(1)一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是______(选填编号).a.c(H2)与c(H2O)的比值保持不变 b....
【简答题】(12分)工业上合成甲醇一般采用下列反应: 下表是该反应在不同温度下的化学平衡常数(K): (1)由表中数据判断 0(填“>”、“=”或“<”)。 (2)某温度下,将2molCO和6molH 2充入2L的密闭容器中,充分反应达到平衡后,测得c(CO)=0.5mol·L -1,则此时的温度为 ℃。 (3)在容积固定的密闭容器中发生上述反应,各物质的浓度如下表: ①反应从2min到4mi...
【单选题】某温度下2L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如表所示.下列说法正确的是( )XYW(起始状态)/mol210(平衡状态)/mol10.51.5
【简答题】(13分)一定条件下发生反应:CO 2 (g)+3H 2 (g) CH 3 OH(g)+H 2 O(g),下图表示该反应进行过程中的能量变化。 (1)图中曲线 (填“a”或“b”)表示使用催化剂时的反应进程。使用催化剂对该反应的影响是______(填选项字母)。 A.提高反应速率 B.提高CO 2 的转化率 C.降低反应活化能 D.改变反应的Δ H (2)CO 2 (g)+3H 2 (g) CH ...
【简答题】(共10分)(1)已知可逆反应:M(g)+N(g)P(g)+Q(g);△H>0,请回答下列问题:①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。(共10分)(1)已知可逆反应:M(g)+N(g)P(g)+Q(g);△H>0,请回答下列问题:①若要增大M的转化率,在其它条件不变的情况下可以采取的措施为_______________。A.加入一定量MB.加入...
【简答题】在恒定温度下反应NH2COONH4(s) 2NH3(g)+CO2(g)达到分解平衡:(1)可以判断该分解反应已经达到化学平衡的是________。 在恒定温度下反应NH2COONH4(s) 2NH3(g)+CO2(g)达到分解平衡:(1)可以判断该分解反应已经达到化学平衡的是________。 A.2v(NH3)=v(CO2) B.密闭容器中总压强不变C.密闭容器中混合气体的密度不变D.密闭容器中...

刷刷题刷刷变学霸